El descubrimiento de la penicilina en 1928 por el Dr. Alexander Fleming supuso un gran avance en la lucha frente a las enfermedades ocasionadas por las bacterias. Dicho aporte propició un ambiente de tranquilidad entre los que se dedicaban al estudio de estas enfermedades, ya que fueron reducidas de manera drástica, aumentando la esperanza de vida en casi 30 años. Debido a esto, los estudios empezaron a centrarse en la investigación de enfermedades víricas, que eran más desconocidas.
Sin embargo, observaron que las enfermedades microbianas ya combatidas volvían a prosperar en la población con mayor virulencia, además de haber disminuido la efectividad de los antibióticos para combatirlos.
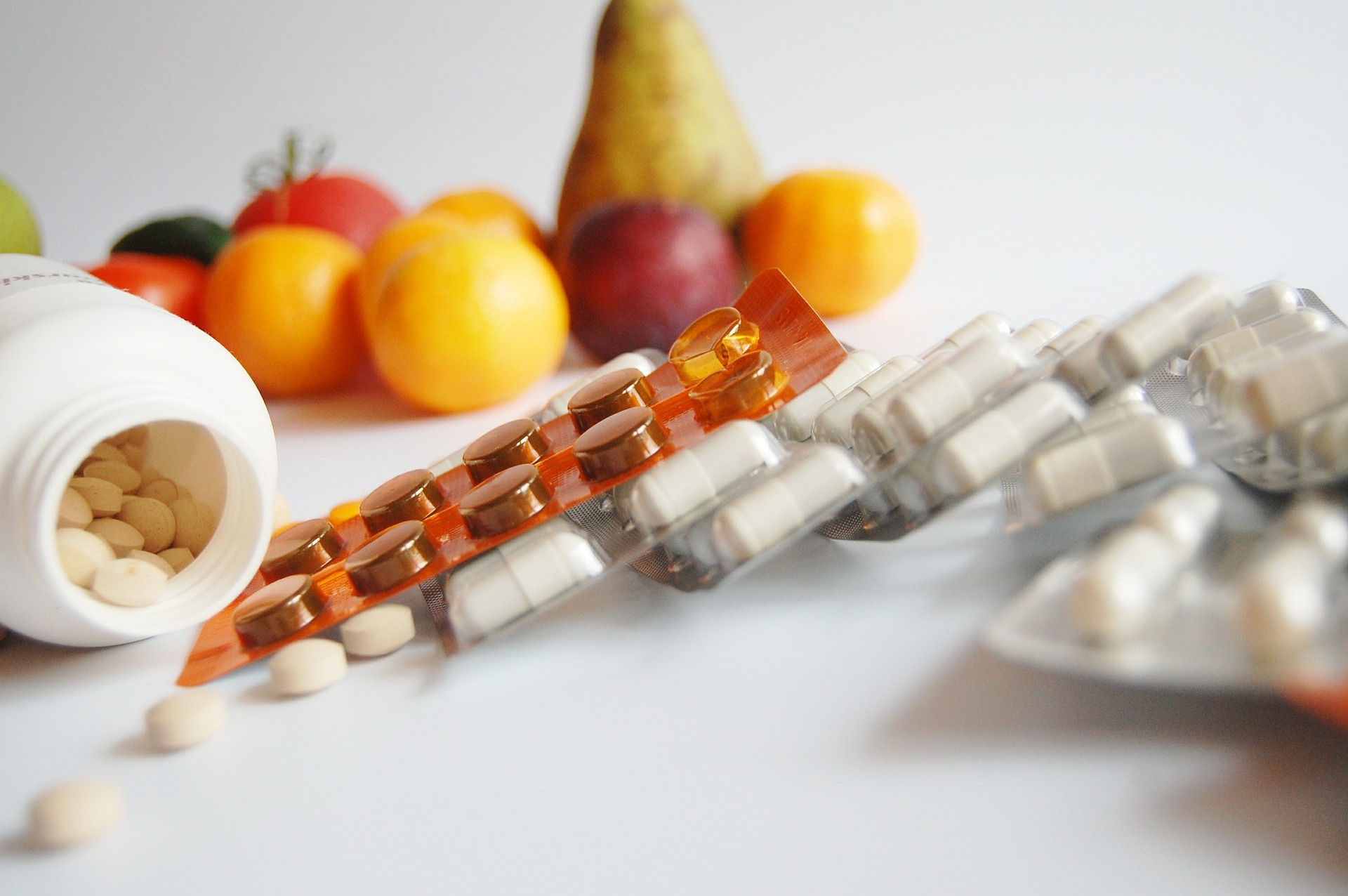
España consume cerca de 700 millones de dosis diarias definidas.
Con ello, se empieza a valorar la posibilidad de que las bacterias obtuvieran resistencia debido a la exposición continua de un microorganismo a un mismo antibiótico. Tal es la severidad del problema que, a día de hoy, se habla de la aparición de bacterias ultrarresistentes con la capacidad de revertir el efecto de cualquier tipo de medicamento que se le suministre. Parte de la culpa se debe al consumo inapropiado y excesivo de estos fármacos sin ser necesario, y a la presencia de mecanismos bacterianos (transducción1, transformación2, transposición3 y conjugación4) que ayudan a la inserción de los genes de resistencia en su plásmido (molécula de ADN circular que se replica independientemente del cromosoma microbiano).
Esto ha obligado a llevar a cabo la búsqueda de alternativas que impidan la proliferación bacteriana en los organismos hospedadores y disminuya su patogenicidad. Una de las opciones más efectivas encontradas hasta ahora ha sido actuar sobre el sistema comunicativo de las bacterias, conocido como quorum sensing. Éste sistema se basa en un conjunto de pequeñas moléculas difusibles (autoinductores) cuya concentración en el medio bacteriano aumenta con su crecimiento, y que alteran la expresión génica al unirse a sus receptores específicos. Así provocan la activación de cascadas de fosforilación y condicionan comportamientos cooperativos como la formación de biofilms, esporulación, toxinas, motilidad o la producción del factor de virulencia. Destacan las N-acil homoserina lactonas en las bacterias Gram negativa y los péptidos en las Gram positiva.
Las N-acil homoserina lactonas, atendiendo a la densidad poblacional, son moléculas capaces de controlar genes determinados al difundir libremente a través de las membranas bacterianas y alcanzar distintos grados de concentración. Como ejemplo se puede observar a la bacteria patógena oportunista Pseudomonas aeruginosa, por su alta producción de metabolitos secundarios dependientes de estas lactonas.
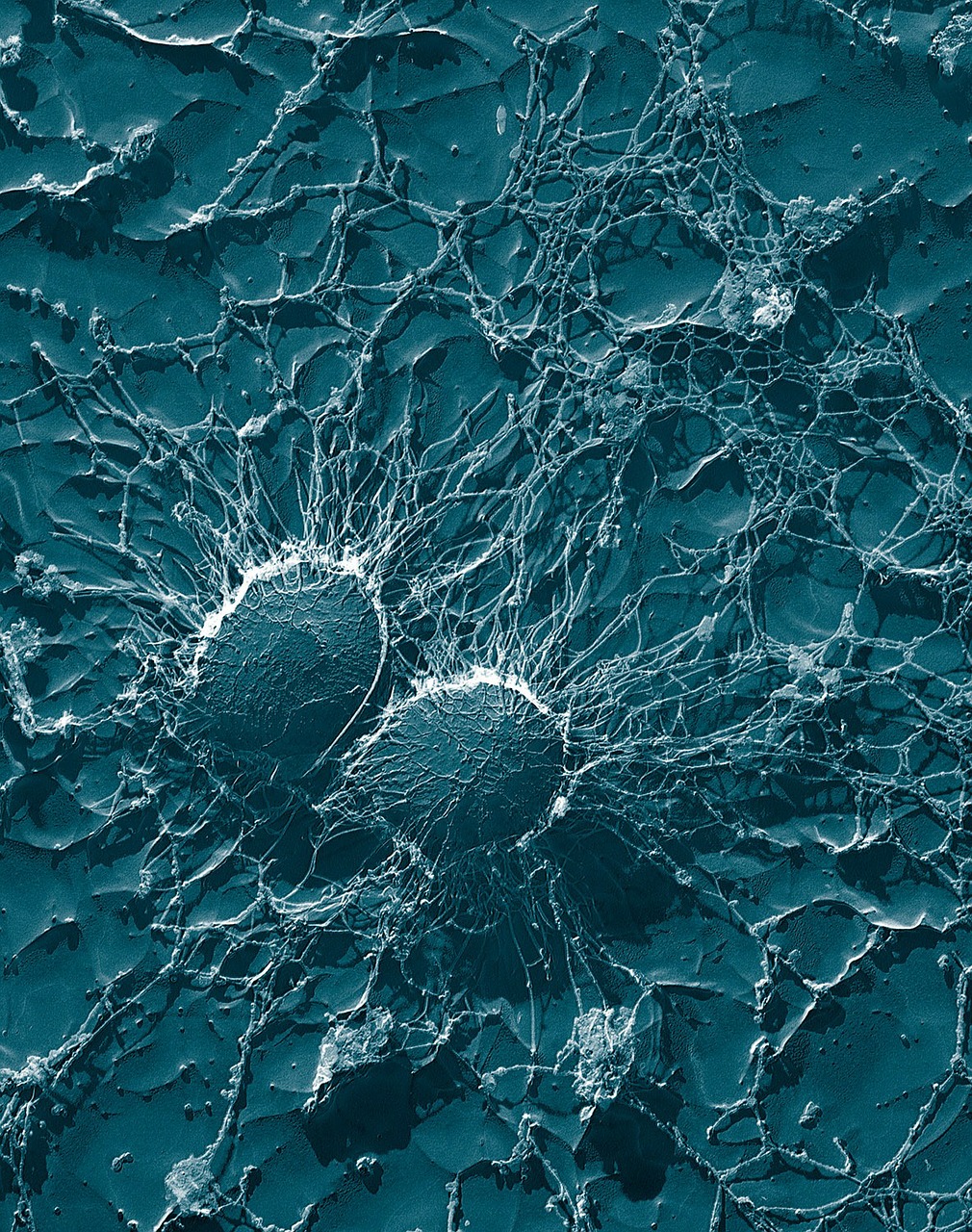
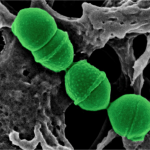
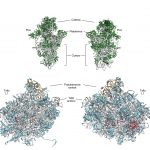
La gran cápsida de la bacteria Staphylococcus aureus le sirve para protegerse frente a los antibióticos
A diferencia de las anteriores, los péptidos de las bacterias Gram positivas son normalmente secretados por transportadores dependientes de ATP (adenosín trifosfato). Algunos de ellos interactúan con receptores sensores quinasa ligados a la membrana que transducen la señal a través de ésta, mientras que otros son transportados al interior por permeasas donde interaccionan con receptores intracelulares. Por ejemplo, la bacteria Staphylococcus aureus aplica este método para la regulación de la formación de factores colonizantes de la superficie celular implicados en su virulencia o, la bacteria Bacillus subtillis para su esporulación.
Por lo tanto, el descubrimiento de inhibidores orientados a actuar sobre el sistema de quorum sensing, es una novedosa estrategia para evitar el consumo indiscriminado de medicamentos y prevenir la aparición de nuevas cepas ultrarresistentes. Dichos compuestos son principalmente de origen vegetal y marino, aunque las propias bacterias los producen para tratar de eliminar a la competencia, ya que funcionan como moléculas antagonistas que compiten por el sitio de unión de los autoinductores de sus respectivos receptores.
Estos agentes bloqueadores del quorum sensing tienen mucho potencial terapéutico como medida profiláctica y abre nuevas líneas de investigación que se originarán conforme se avance en su investigación. Aún así, actualmente, no hay mejor barrera defensiva que nuestro sistema inmunitario para luchar ante cualquier microorganismo exógeno.
Notas
| ↑1 | Transferencia o incorporación de ADN libre extracelular por una bacteria debido a la lisis de otras bacterias. |
|---|---|
| ↑2 | Transferencia de ADN cromosómico o plasmídico de una bacteria a otra por medio de un bacteriófago. |
| ↑3 | Movimiento de una sección de ADN (transposón) que pueden contener genes para la resistencia a antibióticos. |
| ↑4 | Intercambio de material genético entre dos bacterias a través de una hebra sexual o contacto físico. |